Yapay zekâ sistemleri; makine öğrenmesi ve derin öğrenme yöntemleriyle bize hastalığın teşhis ve tedavi sürecinde yardımcı olup en verimli şekilde hekimlik yapabilmemizi sağlamayı vadediyor. Yalnız bizlerden bazı isteklerde bulunuyor ve bu isteklerin başında sisteme analiz etmesi için bol miktarda veri seti sağlanması geliyor. Peki sistem neden veriye ihtiyaç duyuyor?
Sağlık alanında kullanılacak yapay zekâ sistemlerine veri olarak klinik veriler sunulur. Klinik veriler; tanı ve tedavi bilgilerini, reçeteli ilaç bilgilerini, laboratuvar testlerini, fizyolojik monitör verilerini, hastaneye yatış ve hasta sigorta bilgilerini, idari ve demografik bilgileri içerir.
Yapay zekâların doğru analiz yapabilmeleri için eğitim aşamaları boyunca klinikteki verilerin yerini tutacak veri setleri kullanılır ve yapay zekâ, kendisine tek seferde sunulan belirli sayıda ve özellikteki veriyi analiz etmeyi öğrenir. Ardından doğruluk değeri yüksek analizler yapmasında yardımcı olacak yeni verilere sürekli ihtiyaç duyar çünkü yapay zekayı geliştirirken yararlanılan bu örnek veri setlerinin, konuyla ilgili var olan verilerin tümünü kapsaması mümkün değildir.
Sağlık alanında kullanılacak yapay zekâ sistemlerinin eğitilmesi için gerekli verileri karşılayan çalışmalar iki şekilde yapılır. Birincisi, geçmişte elde edilmiş sağlık verilerinin sistemin eğitiminde kullanıldığı “retrospektif” çalışmadır. İkincisi ise farklı giyilebilir cihazlardan veya elektronik sağlık kayıtlarından elde edilen yeni verilerin kullanıldığı “prospektif” çalışmadır. Prospektif çalışmada yapay zekâ sistemi yeni verilerle sürekli eğitilir ve analizlerinin doğruluğu hesaplanır. Peki bu iki çalışma türünden hangisinin yapay zekâ sistemi için tercih edilmesi beklenilir?
Bir yapay zekâ sistemi, retrospektif çalışmalardaki veri setleriyle eğitildikten sonra istenmeyen öğrenme kalıpları oluşturur ve bu, analizlerinde taraflılığa yol açar. Nihayetinde klinikte kullanılmaya başlanan yapay zekâ eğitildiği veri setlerinin içinde bulunmayan verilerle karşılaşınca, yaptığı analizlerin doğruluk oranı istenilen düzeyde kalamaz. Yani sistem asıl amacı olan klinik kullanımda yarar sağlayamaz.
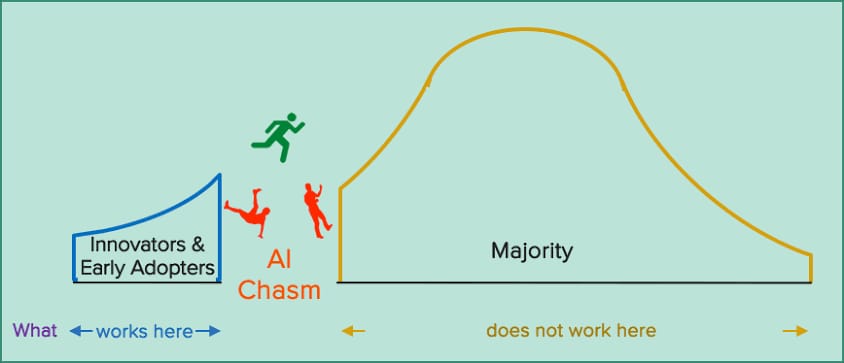
Literatürde buna, “Ai-Chasm” adı verilir. “Ai-Chasm” bizlere, doğruluk oranı yüksek olan bir çalışmanın klinikte her zaman etkinlik gösteremeyeceğini, bunun retrospektif olarak yapılan çalışmanın kendi içinde barındırdığı durağan veri tabanından kaynaklandığını belirtiyor. Bu noktada ihtiyaç duyulan yeni veri setinin düzenli olarak sağlanabilmesi için devreye “prospektif” çalışmalar giriyor. Prospektif çalışmalar, algoritmanın sürekli veri akışıyla eğitilmesine, dolayısıyla yanlış öğrenme kalıplarından kurtulması beklenen yapay zekâ sistemlerinin doğuşuna olanak sağlıyor. Peki literatürde sağlıkta yapay zekâ ile ilgili prospektif ve retrospektif çalışmaların dağılımı nasıl?
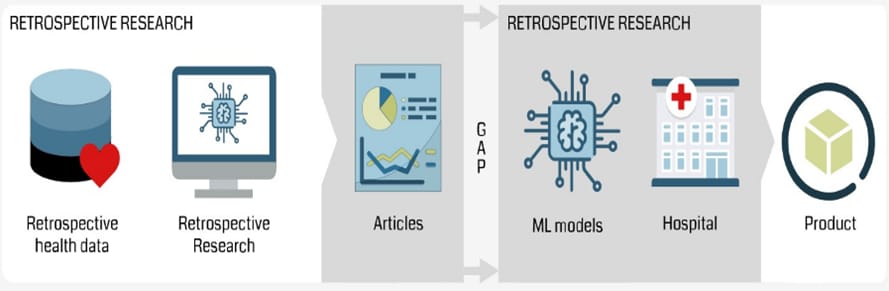
Stanford, Oxford ve Londra Üniversitesi’nden araştırmacıların 81 makaleyi incelediği, Mart 2020’ de yayımlanan çalışmada2 makalelerin prospektif veya retrospektif olarak yürütülme oranına değiniliyor. Hekimlerin ve yapay zekanın yetkinliğini kıyaslamak için geliştirilen derin öğrenme modellerinin sayısı ne kadar artmakta olsa da yayımlanan 81 çalışmanın sadece 9’ unun prospektif ve randomize kontrollü olduğu görülüyor. Diğer taraftan randomize kontrollü olmayan ve retrospektif olan çalışmalar nedeniyle derin öğrenmede taraflılığın artması ve “Ai-Chasm” ın daha da büyümesi söz konusu. Makalede ele alınan 81 derin öğrenme çalışmasının 58 ‘inin taraflılık riski taşıdığı belirtiliyor. Öyleyse literatürde prospektif çalışmaların sayıca arttırılması için neler yapılmalı?
Tam burada devreye sistemin kilit noktasında duran “hekimler” giriyor. Hekimlerin hastalardan giyilebilir cihazlar veya elektronik sağlık kayıtları yoluyla elde ettikleri verileri sürekli ve sistematik bir şekilde kullanması sonucunda, hayati öneme sahip “prospektif” çalışmalar ortaya çıkabiliyor. Bu çalışmalar sayesinde “Ai-Chasm” küçülüyor ve yapay zekâ sistemleri asıl amaçları olan klinik kullanımda etkinlik gösterebilir hale geliyor.
Bu düzenli veri tedarikinin sağlanmasıyla diyabetik retinopatinin derecelendirilmesi3, sentinel lenf nodu biyopsilerinde göğüs kanseri metastazının tespiti4 ve konjenital katarakt tespiti5 için eğitilmiş olan yapay zekaların analizlerinin doğruluk oranı, klinikte istenilen seviyede gözüküyor. Buradan anlaşılacağı üzere yapay zekayı klinikte daha etkin görebilmek “hekimlerin” varlığı ile mümkün.
Teknolojik gelişmelerin klinikte karşılık bulabilmesi için ileri görüşlü hekimlerin, yapay zekâ sistemleri için “multidisipliner bir iş birliği” sağlamaları gerekiyor. Yapay zekaya büyük katkılar sunacak prospektif çalışmaların var olması, biz hekimlerin müdahalesiyle doğrudan ilişkili. Gelecekte böylesi “prospektif” çalışmaların artması ümidiyle.
Sağlıklı günler dilerim.
KAYNAKLAR
1. Kelly, Christopher J et al. “Key challenges for delivering clinical impact with artificial intelligence.” BMC medicine vol. 17,1 195. 29 Oct. 2019, doi:10.1186/s12916-019-1426-2
2. Nagendran, Myura et al. “Artificial intelligence versus clinicians: systematic review of design, reporting standards, and claims of deep learning studies.” BMJ (Clinical research ed.) vol. 368 m689. 25 Mar. 2020, doi:10.1136/bmj.m689
3. Kanagasingam Y, Xiao D, Vignarajan J, Preetham A, Tay-Kearney M-L, Mehrotra A. Evaluation of artificial intelligence-based grading of diabetic retinopathy in primary care. JAMA Netw Open. 2018;1: e182665. https://doi. org/10.1001/jamanetworkopen.2018.2665.
4. Steiner DF, MacDonald R, Liu Y, Truszkowski P, Hipp JD, Gammage C, et al. Impact of deep learning assistance on the histopathologic review of lymph nodes for metastatic breast cancer. Am J Surg Pathol. 2018; 42:1636–46
5. Long E, Lin H, Liu Z, Wu X, Wang L, Jiang J, et al. An artificial intelligence platform for the multihospital collaborative management of congenital cataracts. Nat Biomed Eng. 2017; 1:0024. https://doi.org/10.1038/s41551-016-0024.
6. Cosgriff, Christopher V et al. “The clinical artificial intelligence department: a prerequisite for success.” BMJ health & care informatics vol. 27,1 (2020): e100183. doi:10.1136/bmjhci-2020-100183
7. Mart 6, 2021. “Data Resources in the Health Sciences”. hsl.uw.edu web adresinden elde edildi.
8. Görsel 1. blog.purestorage.com web adresinden elde edildi.
9. Görsel 2. digitalhealth.dk web adresinden elde edildi.


Yanıt yok